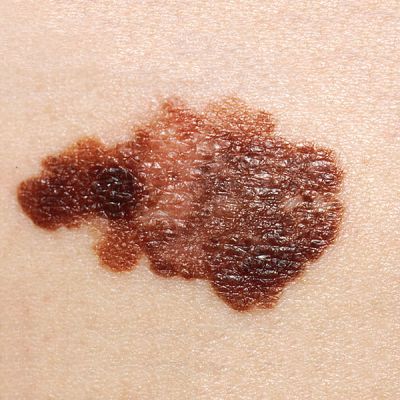
Le mélanome malin
métastatique présente un mauvais pronostic et bien que les inhibiteurs
visant la BRAF mutée aient démontré une efficacité au niveau clinique,
la résistance acquise empêche le potentiel curatif de ces stratégies.
Néanmoins, l'abondance des mutations passagères causées par l'exposition
à la lumière UV complique la découverte de mutations de transformation.
Cherchant à aborder cette question, des scientifiques du projet
MELANOMA GENES («Gene discovery in melanoma progression and therapeutic
resistance»), financé par l'UE, ont utilisé un modèle animal de la
maladie. Cette souris transgénique a accueilli la mutation de protéine
BRAF humaine notamment dans les mélanocytes murins et présenté une
hyperpigmentation de la peau et une formation du mélanome.
La longue latence du déclenchement du cancer au sein de cette souris
a présenté un scénario idéal pour dépister des mutations clés. Les
chercheurs ont élevé cette souris avec la souris porteuse du transposon
de «belle au bois dormant», un élément ADN capable de jongler entre les
positions au sein du génome. Ils ont observé une accélération
significative de tumorigenèse et analysé les sites d'insertion du
transposon afin d'identifier les gènes responsables de cette
observation.
Une liste de gènes avec des rôles établis dans la formation de
mélanome a été établie. Le gène EPC1 (Enhancer of Polycomb 1) était un
des gènes les plus couramment altérés et, étant donnée son implication
dans d'autres cancers, les scientifiques ont décidé d'explorer en
profondeur son rôle de suppresseur de tumeur dans le mélanome. La
suppression de l'expression EPC1 a considérablement affecté la
prolifération et la transformation de la cellule du mélanome.
Par ailleurs, le consortium s'est intéressé à dévoiler les gènes
responsables de la résistance aux médicaments. Dans ce contexte, ils ont
traité les souris atteintes de mélanome avec un inhibiteur BRAF et ont
attendu l'émergence des tumeurs résistantes aux médicaments. Le
séquençage génomique a identifié huit loci génétiques qui ont été mutés à
la suite d'un traitement par médicaments. L'évaluation fonctionnelle de
ces gènes a indiqué l'implication de la voie PI3K dans l'émergence de
la résistance aux médicaments.
Outre fournir un aperçu fondamental dans l'étiologie génétique du
mélanome, les résultats de l'étude MELANOMA GENES ont des implications
cliniques. Ils devraient orienter la recherche et le développement vers
une nouvelle ère de médicaments contre le mélanome avec une efficacité
clinique améliorée et une pharmacorésistance minimale.
 EN
EN CS
CS DE
DE ES
ES FR
FR HU
HU IT
IT PL
PL PT
PT РУ
РУ SK
SK TR
TR УК
УК AR
AR 中文
中文